Promessa o pericolo: serie di problemi relativi al vaccino mRNA contro il COVID-19 (parte 4)
In questa serie, "Promise or Peril: Alarming COVID-19 mRNA Vaccine Issues ", esploriamo come l'introduzione della tecnologia mRNA mancasse di un quadro normativo adeguato, ponendo le basi per eventi avversi gravi e altre preoccupazioni legate a test di sicurezza inadeguati delle nanoparticelle lipidiche , proteine spike e impurità residue correlate al DNA e ai lipidi, nonché specie di mRNA troncate/modificate.
In precedenza: nella Parte 1, abbiamo introdotto come la Food and Drug Administration (FDA) statunitense ha allentato le regole per i vaccini a mRNA rispetto alle terapie a base di mRNA e abbiamo discusso i dati disponibili riguardanti la distribuzione dell'LNP in tutto il corpo sulla base di test sugli animali, il fatto che i test umani erano non è stato fatto e la mancanza di dati sulla biodistribuzione dell'mRNA o delle proteine spike. Nelle parti 2 e 3 abbiamo esplorato come sono costruiti gli LNP e come si comportano nel corpo e influiscono sulla salute.
Passiamo ora a un altro problema: il carico contenuto nelle capsule LNP: l'mRNA e la sua proteina spike codificata. Presentiamo la risposta infiammatoria alla proteina spike e a una delle sue subunità proteiche e il modo in cui possono contribuire a eventi avversi gravi come la miocardite e la coagulazione del sangue.
Rochelle Walensky, ex direttrice dei Centri statunitensi per il controllo e la prevenzione delle malattie (CDC), ha dichiarato su “Good Morning America ” nel giugno 2021 che i casi di miocardite sono “davvero piuttosto rari… lievi, autolimitanti, generalmente si risolvono con il riposo e le normali cure farmaci”. Tuttavia, questa affermazione è stata fatta sulla base di un esame preliminare di 300 casi e prima di condurre un follow-up a lungo termine.
Uno studio pubblicato il 1° agosto ha seguito 40 adolescenti a Hong Kong per un periodo massimo di un anno. Test di follow-up eseguiti su 26 pazienti con risultati iniziali anormali hanno rivelato che il 58% di quelli con miocardite associata al vaccino presentava cicatrici persistenti nel muscolo cardiaco. Gli autori hanno concluso: “Esiste un potenziale effetto a lungo termine sulla capacità di esercizio e sulla riserva funzionale cardiaca durante lo stress”.
Questa serie dimostra come l'esposizione alla proteina spike si traduca in problemi cardiovascolari a valle. Dato che la vaccinazione induce l’organismo a produrre più proteine spike, è chiaro che erano necessarie ulteriori ricerche per comprendere gli impatti sulla salute della vaccinazione prima del rilascio dell’autorizzazione.
Riepilogo dei fatti principali
- La proteina spike del SARS-CoV-2 e la sua subunità S1 hanno effetti noti sul sistema cardiovascolare, come un aumento del rischio di coagulazione del sangue.
- La proteina Spike indotta dal vaccino e la sua subunità S1 sono state trovate nel sangue dopo la vaccinazione.
- Negli studi di laboratorio, la proteina spike attiva i globuli bianchi e può innescare una risposta infiammatoria o una coagulazione.
- La proteina spike libera è stata trovata nel sangue di adolescenti e giovani adulti con miocardite post-mRNA vaccinale, ma non in soggetti sani di controllo senza miocardite.
- La subunità S1 può interagire con ACE2, piastrine e fibrina e può essere ciò che porta a una risposta infiammatoria che determina eventi avversi gravi, tra cui coaguli, miocardite e problemi neurologici.
- Come discusso nella Parte 3, le nanoparticelle lipidiche (LNP) agiscono come adiuvanti, stimolando il sistema immunitario. Questa risposta immunitaria innata raggiunge il picco entro sei ore dalla vaccinazione e ritorna al basale intorno al nono giorno, corrispondente temporalmente all’insorgenza della miocardite, che in genere si verifica entro i primi sette giorni successivi alla vaccinazione con mRNA COVID-19.
- Non sono stati condotti studi per valutare in che modo la vaccinazione influisce su coloro che sono già stati infettati da SARS-CoV-2.
- La proteina spike era implicata nei microcoaguli dei piccoli vasi durante la malattia COVID-19; pertanto, si sarebbero dovuti prevedere gli effetti cardiovascolari post-vaccinazione.
- La prima scadenza per gli studi sulla sicurezza post-autorizzazione imposti dalla FDA è passata, ma per quanto ne sappiamo, il rapporto completo non è stato reso disponibile al pubblico.
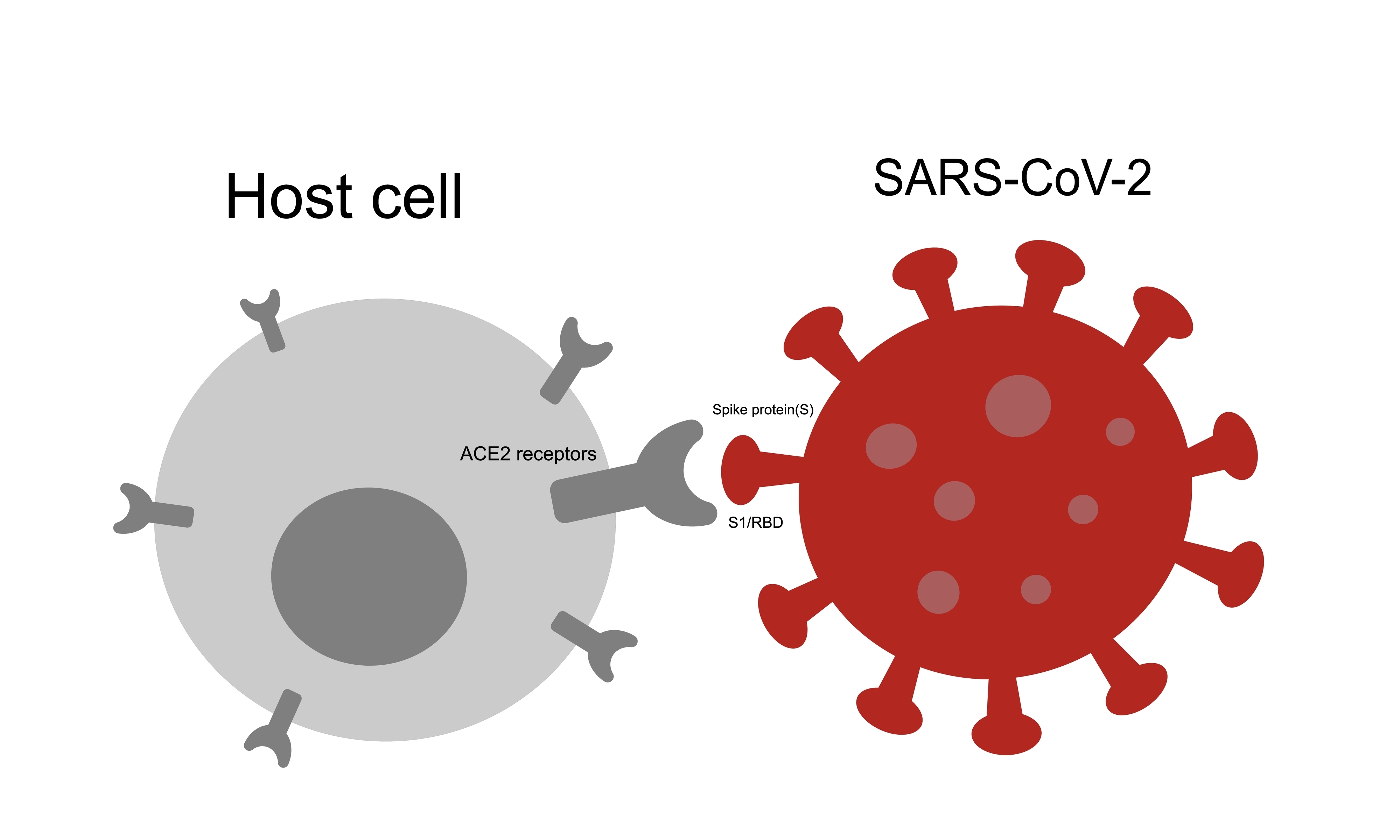
La proteina spike sporge dal virus SARS-CoV-2 come una corona di manici appiccicosi. Il compito della proteina spike è quello di agganciarsi al recettore ACE2 in modo che il virus possa entrare nella cellula. Il recettore ACE2 si trova in molte cellule umane nei polmoni, nei reni, nell’intestino, nel cuore e nel rivestimento dei vasi sanguigni.
La proteina Spike è composta da due parti: le subunità S1 e S2. La proteina della subunità S1 si trova sulla punta della proteina spike ed è responsabile del legame con il recettore ACE2. Una volta legata al recettore, la proteina spike cambia forma per consentire l’ingresso del virus. Avendo avuto accesso all’interno della cellula, il virus SARS-CoV-2 utilizza il processo di produzione delle proteine della cellula per produrre nuove proteine virali.
I vaccini efficaci selezionano antigeni riconoscibili che inducono una risposta immunitaria robusta. La proteina spike è stata scelta per il vaccino mRNA COVID-19 perché è responsabile dell’attaccamento alle cellule e dell’ingresso. Tuttavia, la ricerca suggerisce che la proteina Spike e la sua subunità S1 potrebbero anche essere responsabili di complicanze cardiovascolari a seguito sia dell’infezione che della vaccinazione.
La subunità S2 può anche interferire con la soppressione del tumore , spiegando potenzialmente perché il COVID-19 può essere più grave per i pazienti affetti da cancro.
La ricerca mostra che la proteina spike si trova nel sangue in seguito all’infezione da COVID-19 e alla vaccinazione. La proteina spike modifica la coagulazione del sangue e può stimolare una risposta immunitaria iperattiva. Una migliore comprensione di questi risultati e dei ruoli specifici svolti dalla proteina Spike e dalla sua subunità S1 ci aiuterà a determinare chi è maggiormente a rischio di malattie gravi o di eventi avversi del vaccino.
Effetti cardiovascolari della proteina Spike dopo l'infezione
Sebbene gli studi siano piccoli, la proteina Spike è stata trovata nel sangue e nei coaguli di pazienti affetti da COVID-19 gravemente malati. L’evidenza clinica suggerisce un’impronta digitale degli effetti cardiovascolari della proteina spike.
In uno studio su 41 pazienti pubblicato su Frontiers in Immunology, è stato riscontrato che il 30,4% dei 23 ricoverati in ospedale aveva livelli significativi di proteine spike nella circolazione. Nessuno dei restanti 18 individui non infetti o lievemente malati aveva proteine spike circolanti.
Un piccolo studio caso-controllo ha rilevato la proteina spike nei coaguli recuperati da pazienti COVID-19 con ictus ischemico acuto e infarto miocardico.
Un altro studio ha rilevato la subunità S1 nel plasma del 64% dei pazienti positivi al COVID-19 e i livelli di S1 erano significativamente associati alla gravità della malattia. È stata rilevata anche la proteina nucleocapside (N), un marcatore dell’infezione da COVID-19. Gli autori hanno ipotizzato che la presenza di S1 e N nel plasma suggerisca che frammenti di virus entrino nel flusso sanguigno, potenzialmente a causa di un danno tissutale.
L'esatta catena degli eventi non è completamente compresa. Tuttavia, i risultati di laboratorio, clinici e bioptici offrono prove convergenti che suggeriscono un ruolo della proteina Spike e della sua subunità S1 nella coagulazione del sangue e nelle lesioni cardiache.
Coaguli di sangue associati alla subunità Spike S1
Negli esperimenti di laboratorio come quelli condotti nello studio Frontiers in Immunology, la subunità S1 della proteina spike provoca una reazione a catena che crea le giuste condizioni per la formazione di coaguli. In questa reazione a catena, la proteina S1 si lega al recettore ACE2 sulle cellule che rivestono i vasi sanguigni. Il legame con ACE2 attiva quindi le cellule immunitarie.
Questo effetto domino può anche stimolare il legame delle piastrine, aumentando il rischio di coagulazione. Le piastrine sono agenti coagulanti essenziali che arrestano la perdita di sangue in seguito a lesioni aggregandosi insieme. Gli autori hanno inoltre osservato che in vitro “il nostro gruppo ha recentemente documentato che l’esposizione dei sieri di pazienti affetti da COVID-19 grave alle cellule endoteliali ha indotto l’aggregazione piastrinica”.
In altre parole, la subunità S1 è interessante perché, in vitro (in una provetta), sembra causare cambiamenti nei meccanismi di coagulazione . Se la subunità S1 può influenzare gli agenti della coagulazione come la fibrina, il complemento 3 e la protrombina, questo potrebbe essere un meccanismo attraverso il quale SARS-CoV-2 può causare complicazioni cardiovascolari. La coagulazione provoca cambiamenti nel flusso sanguigno, portando potenzialmente a trombosi, ictus e infarto.
Coaguli di sangue atipici
Fornire anticoagulanti per ridurre il rischio di formazione di coaguli non sembra ridurre il rischio di coagulazione nei pazienti ricoverati o ambulatoriali con COVID-19 . Ciò potrebbe essere dovuto al fatto che i coaguli formati dopo l'esposizione alla subunità S1 potrebbero non essere tipici coaguli di sangue. Tre risultati suggeriscono che la subunità S1 è importante per il rischio di coagulazione.
1. I coaguli resistono alla normale degradazione
Innanzitutto, quando la subunità S1 è stata aggiunta al sangue sano in laboratorio, ha creato depositi di coaguli densi e fibrosi . Questi coaguli fibrosi di “amiloide” si formavano anche quando il sangue prelevato da persone sane veniva esposto alla subunità S1.
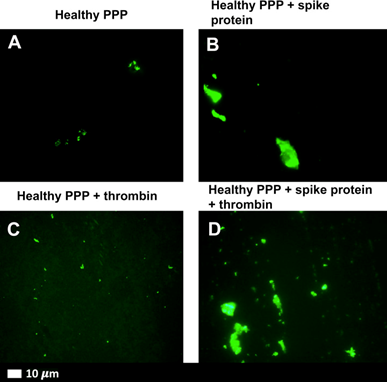
La subunità S1 sembra essere associata alla coagulazione resistente alla fibrinolisi, la normale rottura dei coaguli necessaria per ripristinare il flusso sanguigno dopo un infortunio. Questi coaguli di amiloide sono mostrati nella Figura 1 di seguito.
I coaguli di amiloide si verificano quando una proteina viene danneggiata e inizia a ripiegarsi in modo anomalo su se stessa. Quando queste proteine amiloidi anomale si accumulano nel corpo, possono interferire con la normale funzione.
Figura 1. Coaguli di amiloide formati in risposta alla proteina Spike S1
2. La subunità S1 può indurre sostanze amiloidi
In secondo luogo, questi coaguli densi possono essere causati da alcuni segmenti proteici sulla subunità S1. La proteina Spike ha sette segmenti proteici (peptidi) che possono indurre sostanze fibrose (amiloidi) . Mentre la proteina spike completamente intatta (subunità S1 e S2 attaccate per formare il picco completo) non ha formato questa amiloide, la subunità S1 lo ha fatto. Questa scoperta è interessante perché suggerisce che le subunità della proteina spike possono avere effetti unici sulle cellule.
3. La spike blocca altre proteine che inibiscono la coagulazione
In terzo luogo, le proteine spike possono superare altre proteine, che impediscono la formazione di coaguli. In un altro esperimento di laboratorio progettato per comprendere come si svolge questo processo, gli scienziati hanno scoperto che la proteina spike blocca le proteine importanti per la rottura dei coaguli.
In sintesi, la ricerca in vitro (basata su laboratorio) suggerisce che la subunità S1 della proteina spike può indurre la formazione di coaguli e comprometterne la dissoluzione. Anche se non sappiamo esattamente come questo si traduca nei processi del corpo, Jan Jekielek di Epoch Times ha esplorato la coagulazione e il ruolo delle proteine spike con il patologo Dr. Ryan Cole il 3 giugno e il Dr. Paul Marik il 23 maggio . Nell'intervista, il dottor Cole ha spiegato che la proteina Spike persiste nel corpo più a lungo, infiamma i tessuti ovunque si deposita e agisce come un irritante o una tossina nel corpo.
Proteina Spike trovata in pazienti con miocardite vaccinati con COVID-19
Studi su pazienti vaccinati con COVID-19 con diagnosi di miocardite hanno rilevato proteine spike nel sangue e nei muscoli cardiaci dei pazienti, ma non in quelli senza miocardite.
Trovato nel sangue
La proteina spike a lunghezza intera è stata trovata nel sangue di adolescenti vaccinati con miocardite ma non nel sangue di quelli senza miocardite.
Non è chiaro il motivo per cui la proteina spike circolasse liberamente o non fosse legata dagli anticorpi. Gli adolescenti che hanno sviluppato miocardite avevano marcatori immunitari simili a quelli che non hanno sviluppato miocardite. In altre parole, il gruppo con miocardite non sembrava avere problemi immunitari.
Piuttosto, questi adolescenti potrebbero aver avuto una risposta immunitaria naturale iperattiva. Una forte immunità naturale (“innata”) aiuta il corpo a combattere le malattie senza alcuna esposizione precedente. Tuttavia, i primi soccorritori (citochine infiammatorie) possono talvolta essere esuberanti. Se la risposta immunitaria innata reagisce in modo eccessivo, può scatenare la miocardite.
Trovato nel muscolo cardiaco
La proteina spike codificata dall'mRNA è stata trovata anche nelle cellule del muscolo cardiaco. È stato condotto uno studio di biopsia endomiocardica (muscolo cardiaco) su 15 pazienti con miocardite in seguito alla vaccinazione. Non è stata riscontrata alcuna altra infezione virale che possa aver causato la miocardite.
I ricercatori hanno trovato la proteina picco SARS-CoV-2 in nove dei 15 pazienti. Nei campioni bioptici sono state rilevate anche cellule immunitarie (CD4+ T). Queste osservazioni suggeriscono una reazione infiammatoria alla proteina spike.
Gli autori hanno concluso: “Sebbene non sia possibile stabilire una relazione causale tra la vaccinazione e l’insorgenza di infiammazione del miocardio sulla base dei risultati, il rilevamento cardiaco della proteina spike, l’infiammazione dominata dalle cellule T CD4+ e la stretta relazione temporale sostengono la necessità di un vaccino -reazione autoimmune innescata.
Uno studio di modellizzazione del 2022 suggerisce anche che la proteina spike può causare una risposta autoimmune imitando le molecole umane, facendo sì che gli anticorpi si leghino alle proteine “self”.
Spike S1 rilevato nel sangue di adulti vaccinati
Un altro studio ha rilevato che 11 adulti su 13 vaccinati con l’mRNA-1273 di Moderna avevano la subunità S1 nel sangue già un giorno dopo la vaccinazione.
Il plasma è stato raccolto da 13 partecipanti in momenti diversi durante il primo mese dopo ciascuna dose. Gli antigeni S1 e il picco sono stati misurati per stimare la quantità di traduzione dell'mRNA in prodotti proteici.
Dopo la prima dose da 100 microgrammi, l'antigene S1 è stato rilevato nel plasma di 11 partecipanti. Al contrario, l’antigene del picco è stato rilevato in tre dei 13 partecipanti. Il picco dell'antigene S1 è stato rilevato in media cinque giorni dopo la vaccinazione. Ancora una volta, la tempistica di questo picco per S1 sembra aggiungere indizi che suggeriscono una risposta autoimmune nella settimana successiva alla vaccinazione.
mRNA rilevato nel sangue e nei linfonodi dopo la vaccinazione
Anche l’mRNA del vaccino, che codifica per la proteina “spike” e la sua subunità S1, persiste nel sangue e nei linfonodi. Dopo la vaccinazione, l'mRNA codificato dal picco è stato trovato nel sangue per 15 giorni e nei linfonodi fino a 60 giorni. Sono stati trovati esosomi carichi di punte circolanti nel sangue per un massimo di quattro mesi. Questa scoperta è importante perché confuta l'affermazione del CDC secondo cui l'mRNA è così fragile da dissolversi rapidamente nel sito di iniezione (vedere Figura 2a nella Parte 1 ).
I linfonodi continuano a creare anticorpi più adatti dopo qualsiasi infezione virale. Questo è un modo fondamentale in cui i nostri corpi si preparano naturalmente a nuove varianti. Tuttavia, livelli persistentemente elevati di mRNA e di proteine spike indotti dal vaccino potrebbero non essere utili quando viene chiesto al sistema immunitario di rispondere a varianti future. In altre parole, se il sistema immunitario ha il compito di continuare a produrre anticorpi contro una variante precedente, potrebbe essere meno agile quando gli viene chiesto di creare un anticorpo di alta qualità per una nuova variante.
Studi clinici inadeguati lasciano domande irrisolte
Dato ciò che sappiamo sugli effetti dannosi del virus SARS-CoV-2, non avremmo dovuto presumere che la proteina spike codificata dal vaccino sarebbe stata innocua.
E, dato ciò che sappiamo sui problemi di coagulazione successivi all’infezione da COVID-19, gli studi futuri dovrebbero verificare se anche la subunità S1 prodotta in risposta alla vaccinazione può causare problemi di coagulazione attraverso lo stesso percorso. Questi studi dovrebbero includere sia esperimenti di laboratorio che osservazioni umane.
Inoltre, non conosciamo le quantità relative di proteine spike libere in circolazione a seguito dell’infezione rispetto alla vaccinazione.
Nel caso dei vaccini contro il Covid-19, il principio attivo non è stato studiato prima dell’autorizzazione. I produttori hanno utilizzato l’mRNA che codifica per una proteina sostitutiva (luciferasi) per testare la sicurezza e la biodistribuzione dei vaccini mRNA.
Pfizer ha presentato dati sulla biodistribuzione animale alle agenzie di regolamentazione utilizzando la codifica dell'RNA surrogato per la luciferasi, come discusso nella Parte 1 di questa serie.
Tuttavia, questi studi erano inadeguati nel descrivere come l’mRNA, la proteina spike, la sua subunità S1 e il trasportatore LNP avrebbero influenzato il corpo umano.
In questo articolo, abbiamo descritto i risultati di laboratorio che mostrano la coagulazione associata alla subunità S1. Studi come questi rafforzano il motivo per cui studi preclinici approfonditi sono così cruciali. Gli studi condotti dalle aziende farmaceutiche non sono stati sufficienti per rispondere a queste domande.
Avevamo pochissime informazioni su come le persone avrebbero risposto alla vaccinazione a seconda dell’età, del sesso, dello stato immunitario, della salute generale o della storia di precedente infezione da SARS-CoV-2. Gli studi clinici originali non hanno arruolato un numero sufficiente di persone già guarite da COVID-19; non erano progettati per fornire una comprensione di come una precedente infezione avrebbe influenzato la risposta di una persona alla vaccinazione.
Lo studio sulla sicurezza post-autorizzazione richiesto da Pfizer non è disponibile al pubblico
Gli studi pre-autorizzazione erano chiaramente inadeguati. Dopo l’autorizzazione, la FDA ha riconosciuto solo che la sorveglianza passiva è insufficiente per stabilire la sicurezza. L’agenzia ha risposto alle segnalazioni di eventi avversi richiedendo a Pfizer di condurre ulteriori studi, con il primo rapporto di monitoraggio previsto per ottobre 2022.
A pagina 6 della lettera di approvazione , la FDA riconosce questo fatto (vedere la Figura 2 di seguito):
“Abbiamo stabilito che un’analisi degli eventi avversi postmarketing spontanei riportati nella sezione 505(k)(1) della FDCA non sarà sufficiente per valutare i rischi gravi noti di miocardite e pericardite e identificare un rischio grave inaspettato di miocardite subclinica.
“Inoltre, il sistema di farmacovigilanza che la FDA è tenuta a mantenere ai sensi della sezione 505(k)(3) della FDCA non è sufficiente per valutare questi gravi rischi. Pertanto, sulla base di dati scientifici appropriati, abbiamo stabilito che è necessario che lei conduca i seguenti studi. …”
La FDA ha ricevuto il rapporto di monitoraggio di Pfizer , previsto entro il 31 ottobre 2022? Il prossimo rapporto, il rapporto intermedio, sarà presentato a ottobre.
Figura 2. Requisiti dello studio sulla sicurezza post-marketing della FDA

Leggi la Parte 1: Necessaria una revisione della FDA per i nuovi vaccini e le terapie mRNA
Leggi la Parte 2: Implicazioni sulla salute degli scadenti test dell'mRNA del COVID-19: aborto spontaneo, perdita della vista, immunotossicità
Successivo: Nella Parte 5, discuteremo i problemi di produzione dell'mRNA che influenzano la contaminazione con DNA a doppio filamento e il potenziale di integrazione del genoma.
Fonte: qui
◊ Riferimenti
Addgene. Riferimento alla biologia molecolare. https://www.addgene.org/mol-bio-reference/#introduction
Alana F Ogata, Chi-An Cheng, Michaël Desjardins, Yasmeen Senussi, Amy C Sherman, Megan Powell, Lewis Novack, Salena Von, Xiaofang Li, Lindsey R Baden, David R Walt, Sindrome respiratoria acuta grave circolante da coronavirus 2 (SARS-CoV) -2) Antigene del vaccino rilevato nel plasma dei destinatari del vaccino mRNA-1273, Clinical Infectious Diseases, Volume 74, Numero 4, 15 febbraio 2022, Pagine 715–718, https://doi.org/10.1093/cid/ciab465
Aldén M, Olofsson Falla F, Yang D, Barghouth M, Luan C, Rasmussen M, De Marinis Y. Trascrizione inversa intracellulare del vaccino mRNA BNT162b2 di Pfizer BioNTech COVID-19 in vitro nella linea cellulare del fegato umano. Curr Problemi Mol Biol. 25 febbraio 2022;44(3):1115-1126. doi: 10.3390/cimb44030073. PMID: 35723296; ID PMC: PMC8946961. https://pubmed.ncbi.nlm.nih.gov/35723296/
Reazioni allergiche inclusa anafilassi dopo la ricezione della prima dose del vaccino Pfizer-BioNTech COVID-19 - Stati Uniti, 14–23 dicembre 2020. MMWR Morb Mortal Wkly Rep 2021;70:46–51. DOI: http://dx.doi.org/10.15585/mmwr.mm7002e1
Anderson EJ, Rouphael NG, Widge AT et al. Sicurezza e immunogenicità del vaccino SARS-CoV-2 mRNA-1273 negli anziani N Engl J Med 2020; 383:2427-2438 https://www.nejm.org/doi/full/10.1056/NEJMoa2028436
Anderson S. Piani CBER per il monitoraggio della sicurezza e dell’efficacia del vaccino COVID-19. https://stacks.cdc.gov/view/cdc/97349 20 ottobre 2020. Accesso 20/03/23.
Angeli F, Spanevello A, Reboldi G, Visca D, Verdecchia P. Vaccini SARS-CoV-2: Luci e ombre. Eur J Intern Med. 2021 giugno;88:1-8. doi: 10.1016/j.ejim.2021.04.019. Epub 2021 30 aprile. PMID: 33966930; ID PMC: PMC8084611. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8084611/#bib0043
Baker, AT, Boyd, RJ, Sarkar, D., Teijeira-Crespo, A., Chan, CK, Bates, E., Waraich, K., Vant, J., Wilson, E., Truong, CD, Lipka- Lloyd, M., Fromme, P., Vermaas, J., Williams, D., Machiesky, L., Heurich, M., Nagalo, BM, Coughlan, L., Umlauf, S., Chiu, PL, … Borad , MJ (2021). ChAdOx1 interagisce con CAR e PF4 con implicazioni per la trombosi con sindrome trombocitopenica. Progressi della scienza. 7(49), eabl8213. https://doi.org/10.1126/sciadv.abl8213
Baumeier C, Aleshcheva G, Harms D, Gross U, Hamm C, Assmus B, Westenfeld R, Kelm M, Rammos S, Wenzel P, Münzel T, Elsässer A, Gailani M, Perings C, Bourakkadi A, Flesch M, Kempf T , Bauersachs J, Escher F, Schultheiss HP. Infiammazione intramiocardica dopo la vaccinazione COVID-19: una serie di casi comprovati dalla biopsia endomiocardica. Giornale internazionale di scienze molecolari. 2022; 23(13):6940. https://doi.org/10.3390/ijms23136940
Bloom, K., van den Berg, F. & Arbuthnot, P. Vaccini a RNA autoamplificanti per malattie infettive. Gene Ther 28, 117–129 (2021). https://doi.org/10.1038/s41434-020-00204-y. https://www.nature.com/articles/s41434-020-00204-y
Chauhan, H., Mohapatra, S., Munt, DJ et al. Considerazioni sulla caratterizzazione fisico-chimica e sulla formulazione delle nanoparticelle lipidiche solide. AAPS PharmSciTech 17, 640–651 (2016). https://doi.org/10.1208/s12249-015-0394-x
Chui CSL, Fan M, Wan EYF, et al. Eventi tromboembolici e ictus emorragico dopo vaccinazione COVID-19 con mRNA (BNT162b2) e inattivata (CoronaVac): uno studio di casi autocontrollati. Lancetta. 2022;(50). https://www.thelancet.com/journals/eclinm/article/PIIS2589-5370(22)00234-6/fulltext
Dag Berild J, Bergstad Larsen V, Myrup Thiesson E, et al. Analisi degli eventi tromboembolici e trombocitopenici dopo i vaccini COVID-19 AZD1222, BNT162b2 e MRNA-1273 in 3 paesi nordici. JAMA Rete aperta. 2022;5(6):e2217375. doi:10.1001/jamanetworkopen.2022.17375 https://jamanetwork.com/journals/jamanetworkopen/fullarticle/2793348
da Silva RL. Microangiopatie trombotiche associate a virus. Ematologia/Oncologia e terapia con cellule staminali. 2011:4(2):51-59. https://www.sciencedirect.com/science/article/pii/S165838761150038X
De A, Ko YT. Perché le formulazioni di LNP ionizzabili con mRNA hanno vita così breve: cause e via d'uscita. Opinione degli esperti Consegna farmaci 2023 febbraio;20(2):175-187. doi: 10.1080/17425247.2023.2162876. Epub 2023 gennaio 1. PMID: 36588456. https://pubmed.ncbi.nlm.nih.gov/36588456/
Ehaideb, SN, Abdullah, ML, Abuyassin, B. et al. Prova di un ampio divario tra COVID-19 negli esseri umani e nei modelli animali: una revisione sistematica. Critica Cura 24, 594 (2020). https://doi.org/10.1186/s13054-020-03304-8
Agenzia europea per i medicinali https://www.ema.europa.eu/en/documents/assessment-report/comirnaty-epar-public-assessment-report_en.pdf
Faizullin D, Valiullina Y, Salnikov V, Zuev Y. L'interazione diretta del fibrinogeno con microparticelle lipidiche modula la cinetica della coagulazione e la struttura del coagulo. Nanomedicina. 2020 gennaio;23:102098. doi: 10.1016/j.nano.2019.102098. Epub 23 ottobre 2019. PMID: 31655206. https://pubmed.ncbi.nlm.nih.gov/31655206/
FDA. Considerazioni sugli studi sul bilancio di massa radiomarcato sull'uomo – Guida per l'industria. https://www.fda.gov/media/158178/download maggio 2022.
FDA. Sviluppo e autorizzazione dei vaccini per prevenire il COVID-19. https://www.fda.gov/media/139638/download
Approvazione FDA-CBER-2021-5683-0013962 il: 09-nov-2020. Uno studio sulla distribuzione nei tessuti di una formulazione di nanoparticelle lipidiche-mRNA marcate con [3H] contenente ALC-0315 e ALC-0159 dopo somministrazione intramuscolare nei ratti Wistar Han. RAPPORTO FINALE Studio della struttura di test n. 185350 N. di riferimento dello sponsor ALC-NC-0552 https://phmpt.org/wp-content/uploads/2022/03/125742_S1_M4_4223_185350.pdf
Fertig TE, Chitoiu L, Marta DS, Ionescu VS, Cismasiu VB, Radu E, Angheluta G, Dobre M, Serbanescu A, Hinescu ME, Gherghiceanu M. L'mRNA del vaccino può essere rilevato nel sangue a 15 giorni dopo la vaccinazione. Biomedicine. 2022 giugno 28;10(7):1538. doi: 10.3390/biomedicines10071538. PMID: 35884842; ID PMC: PMC9313234. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9313234/
Grobbelaar LM et al. La proteina S1 del picco SARS-CoV-2 induce la fibrina (ogeno) resistente alla fibrinolisi: implicazioni per la formazione di microcoaguli in COVID-19 Biosci Rep (2021) 41 (8): BSR20210611. https://doi.org/10.1042/BSR20210611
Hou, X., Zaks, T., Langer, R. et al. Nanoparticelle lipidiche per il rilascio di mRNA. Nat Rev Mater 6, 1078–1094 (2021). https://doi.org/10.1038/s41578-021-00358-0
Iaboni A, Jindal N, Betschel SD, Song C. Sicurezza del vaccino mRNA COVID-19 della seconda dose in pazienti con reazioni immediate dopo la prima dose: una serie di casi. Giornale di allergia e immunologia clinica: globale. 2022;1(3): 172-174. https://www.sciencedirect.com/science/article/pii/S2772829322000200
Parliamo di nanoparticelle lipidiche. Nat Rev Mater 6, 99 (2021). https://www.nature.com/articles/s41578-021-00281-4
Li, JX., Wang, YH., Bair, H. et al. Valutazione del rischio di occlusione vascolare retinica dopo la vaccinazione COVID-19. npj Vaccini 8, 64 (2023). https://doi.org/10.1038/s41541-023-00661-7
Michieletto, D., Lusic, M., Marenduzzo, D. et al. Principi fisici dell'integrazione retrovirale nel genoma umano. Nat Commun 10, 575 (2019). https://doi.org/10.1038/s41467-019-08333-8
Moghimi, SM e Simberg, D. (2022). Preoccupazioni pro-infiammatorie con le nanoparticelle lipidiche. Terapia molecolare: The Journal of the American Society of Gene Therapy, 30(6), 2109–2110. https://doi.org/10.1016/j.ymthe.2022.04.011
Podcast di ispirazione naturale. Jessica Rose PhD – VAERS, dati e verità https://www.audible.com/pd/Jessica-Rose-PhD-VAERS-Data-And-Truth-Podcast/B09YMLJGBN?clientContext=132-5166709-6339436&loginAttempt=true&noChallengeShown=true
Nunez-Castilla J, Stebliankin V, Baral P, Balbin CA, Sobhan M, Cickovski T, Mondal AM, Narasimhan G, Chapagain P, Mathee K, et al. Potenziale autoimmunità derivante dal mimetismo molecolare tra il picco SARS-CoV-2 e le proteine umane. Virus. 2022; 14(7):1415. https://doi.org/10.3390/v14071415
Nyström S, Hammarström P. Amiloidogenesi della proteina Spike SARS-CoV-2. Marmellata. Chimica. Soc. 2022, 144, 20, 8945–8950. https://pubs.acs.org/doi/10.1021/jacs.2c03925
Ogata AF, Maley AM, Wu C, et al. Profilazione seriale ultrasensibile di antigeni e anticorpi SARS-CoV-2 nel plasma per comprendere la progressione della malattia nei pazienti affetti da COVID-19 con malattia grave, Chimica clinica, volume 66, numero 12, dicembre 2020, pagine 1562–1572, https: // doi.org/10.1093/clinchem/hvaa213
La produzione di Ohlson J. Plasmid è il collo di bottiglia della rivoluzione della medicina genetica. Scoperta della droga oggi. 16 ottobre 2020;25(11):1891–3. doi: 10.1016/j.drudis.2020.09.040. Epub prima della stampa. PMID: 33075470; ID PMC: PMC7564888. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7564888/
Perico L, Marina Morigi M, Galbusera M, et al. La proteina 1 della punta SARS-CoV-2 attiva le cellule endoteliali microvascolari e il sistema del complemento portando all'aggregazione piastrinica. Davanti. Immunolo. 2022 https://www.frontiersin.org/articles/10.3389/fimmu.2022.827146/full
Qin, S., Tang, X., Chen, Y. et al. Terapie basate sull'mRNA: strumenti potenti e versatili per combattere le malattie. Sig Transduct Target Ther 7, 166 (2022). https://doi.org/10.1038/s41392-022-01007-w
Rafati A, Pasebani Y, Jameie M, et al. Associazione tra vaccinazione o infezione SARS-CoV-2 con paralisi di Bell: una revisione sistematica e una meta-analisi. JAMA Otorinolaringoiatria Testa Collo Chirurg. Pubblicato online il 27 aprile 2023. doi:10.1001/jamaoto.2023.016 https://jamanetwork.com/journals/jamaotolaryngology/fullarticle/2804297
Rhea EM, Logsdon AF, Hansen KM, Williams LM, Reed MJ, Baumann KK, Holden SJ, Raber J, Banks WA, Erickson MA. La proteina S1 di SARS-CoV-2 attraversa la barriera emato-encefalica nei topi. Nat Neurosci. 2021 marzo;24(3):368-378. doi: 10.1038/s41593-020-00771-8. Epub 2020 16 dicembre. PMID: 33328624; ID PMC: PMC8793077. https://pubmed.ncbi.nlm.nih.gov/33328624/
Röltgen K, Nielsen SCA, Silva O. Imprinting immunitario, ampiezza del riconoscimento delle varianti e risposta del centro germinale nell'infezione e nella vaccinazione umana SARS-CoV-2. Cella 2022;185(6):1025-1040. https://www.cell.com/cell/fulltext/S0092-8674(22)00076-9
Rosenblum HG, Gee J, Liu R, et al. Sicurezza dei vaccini mRNA somministrati durante i primi 6 mesi del programma di vaccinazione statunitense contro il COVID-19: uno studio osservazionale sulle segnalazioni al Vaccine Adverse Event Reporting System e a v-safe. Malattie infettive della lancetta. 2022;22(6):802-812. https://doi.org/10.1016/S1473-3099(22)00054-8
Schmeling, M, Manniche, V, Hansen, PR. Sicurezza dipendente dal lotto del vaccino BNT162b2 mRNA COVID-19. Eur J Clin Invest. 2023; 00:e13998. doi:10.1111/eci.13998. https://pubmed.ncbi.nlm.nih.gov/36997290/
Singh N, la subunità Bharara Singh A. S2 di SARS-nCoV-2 interagisce con la proteina soppressore del tumore p53 e BRCA: uno studio in silico. Trad. Oncol. 2020 ottobre;13(10):100814. doi: 10.1016/j.tranon.2020.100814 . Epub 2020 30 giugno. PMID: 32619819; ID PMC: PMC7324311.
Srinivasan M, Thangaraj SR, Arzoun H. Terapia genica: può curare il diabete di tipo 1? Cureo. 2021 dic 19;13(12):e20516. doi: 10.7759/cureus.20516. PMID: 35004071; ID PMC: PMC8723777. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8723777/
Trougakos IP, Terpos E, Alexopoulos H, et al. Effetti avversi dei vaccini a mRNA COVID-19: l’ipotesi del picco. Cella 2022;28(7): P542-554. https://www.cell.com/trends/molecular-medicine/fulltext/S1471-4914(22)00103-4
Vervaeke P, Borgos SE, Sanders NN, Combes F. Linee guida normative e strumenti preclinici per studiare la biodistribuzione delle terapie a base di RNA. Adv Drug Deliv Rev. 2022 maggio;184:114236. doi: 10.1016/j.addr.2022.114236. Epub 26 marzo 2022. PMID: 35351470; ID PMC: PMC8957368. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8957368/
Wong DWL, Klinkhammer BM, Djudjaj S, Villwock S, Timm MC, Buhl EM, Wucherpfennig S, Cacchi C, Braunschweig T, Knüchel-Clarke R, Jonigk D, Werlein C, Bülow RD, Dahl E, von Stillfried S, Boor P Tropismo cellulare multisistemico della SARS-CoV-2 nelle autopsie di pazienti affetti da COVID-19. Celle. 27 luglio 2021;10(8):1900. doi: 10.3390/cells10081900. PMID: 34440669; ID PMC: PMC8394956. https://pubmed.ncbi.nlm.nih.gov/34440669/
Yonker LM, Swank Z, Bartsch YC et al. Proteina Spike circolante rilevata nella miocardite da vaccino mRNA post-COVID-19. Circolazione. 2023:147(11). https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.122.061025
Yu CK, Tsao S, Ng CW, Chua GT, Chan KL, Shi J, Chan YY, Ip P, Kwan MY, Cheung YF. Valutazione cardiovascolare fino a un anno dopo la miocardite associata al vaccino COVID-19. Circolazione. 2023 agosto;148(5):436-439. doi: 10.1161/CIRCULATIONAHA.123.064772 . Epub 2023 31 luglio. PMID: 37523760; ID PMC: PMC10373639.
Zheng Y, Zhao J, Li J, Guo Z, Sheng J, Ye X, Jin G, Wang C, Chai W, Yan J, Liu D, Liang X. La proteina del picco SARS-CoV-2 causa la coagulazione del sangue e la trombosi attraverso la competizione legandosi all'eparan solfato. Int J Biol Macromol. 15 dicembre 2021;193(Pt B):1124-1129. doi: 10.1016/j.ijbiomac.2021.10.112. Epub 29 ottobre 2021. PMID: 34743814; ID PMC: PMC8553634. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8553634/

Nessun commento:
Posta un commento